研究組織・メンバー
A02:視床下部ー中隔核ー海馬の多領域連関による睡眠覚醒状態依存的脳情報動態変化
 研究代表者
研究代表者
山中章弘・名古屋大学環境医学研究所・教授
WEBhttp://www.riem.nagoya-u.ac.jp/4/drof1/nr/index.html
紹介文本文
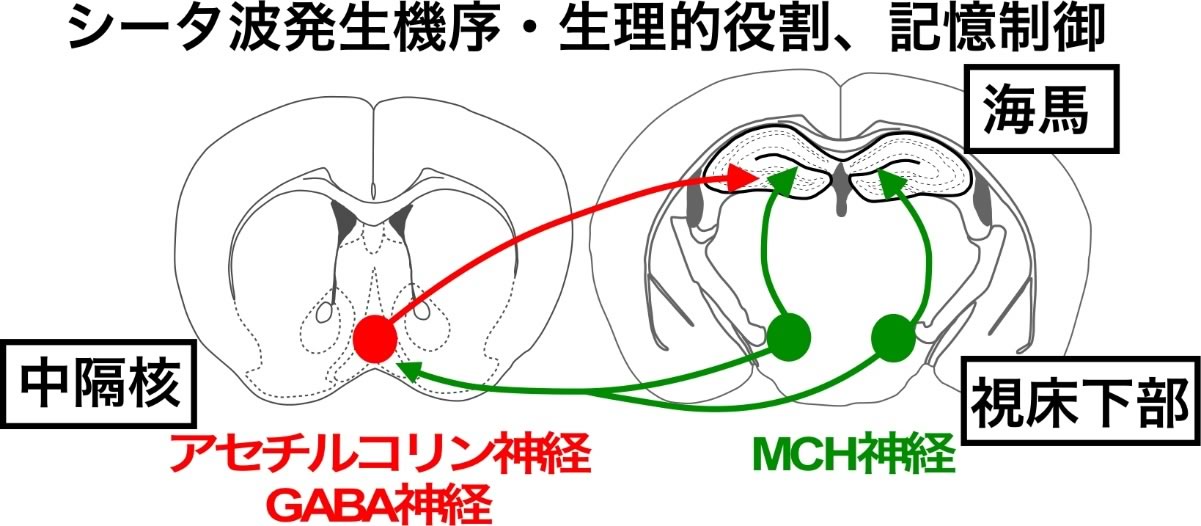
視床下部のメラニン凝集ホルモン(MCH)神経は、睡眠中に活動し、特にレム睡眠中に高い活動を示す。MCH神経は、幅広い脳領域に投射しているが、海馬と中隔核に特に密に投射しており、睡眠中に視床下部-海馬-中隔核において何らかの機能連関が想定されている。これまでにMCH神経を脱落させると記憶形成が向上すること、逆に光遺伝学や薬理遺伝学を用いて活性化すると、レム睡眠時間が有意に増加して記憶を抑制・消去する作用があることを見いだしている。一方、中隔核のアセチルコリン作動性神経も、海馬に密に投射しており、海馬におけるシータ波生成に関わっているとされている。アセチルコリン作動性神経特異的にCreリコンビナーゼを発現するChAT-Creマウスと、Cre依存的にジフテリアトキシンを発現するアデノ随伴ウイルスベクターを用いて、中隔核のアセチルコリン作動性神経を脱落させると、レム睡眠時間とレム睡眠時のシータ波成分が減少しMCH神経脱落と同様の記憶形成の向上が認められたことから、視床下部-中隔核-海馬間において、何らかの機能連関が存在し、睡眠覚醒状態に応じた記憶の調節が行われている可能性が示唆された。本研究では、同領域間の神経回路の動作原理を解明し、また、海馬シータ波の発生機序やレム睡眠の生理的役割についても検討を行う。睡眠覚醒状態に応じた海馬の脳情報動態の変化について明らかにすることで、脳情報の圧縮貯蔵という過程を理解し、脳情報動態学の確立に寄与することを目的としている。
文献
- Chowdhury S, *Yamanaka A. (2016)
Optogenetic activation of serotonergic terminals facilitates GABAergic inhibitory input to orexin/hypocretin neurons.
Sci Rep. 6: 36039. - Tabuchi S, Tsunematsu T, Black SW, Tominaga M, Maruyama M, Takagi K, Minokoshi Y, Sakurai T, *Kilduff TS, *Yamanaka A. (2014)
Conditional ablation of orexin/hypocretin neurons: A new mouse model for the study of narcolepsy and orexin system function.
J Neurosci. 34(19): 6495-6509. - Tsunematsu T, Ueno T, Tabuchi S, Inutsuka A, Tanaka KF, Hasuwa H, Kilduff TS, Terao A, *Yamanaka A. (2014)
Optogenetic manipulation of activity and temporally-controlled cell-specific ablation reveal a role for MCH neurons in sleep/wake regulation.
J Neurosci. 34(20): 6896-6909.


